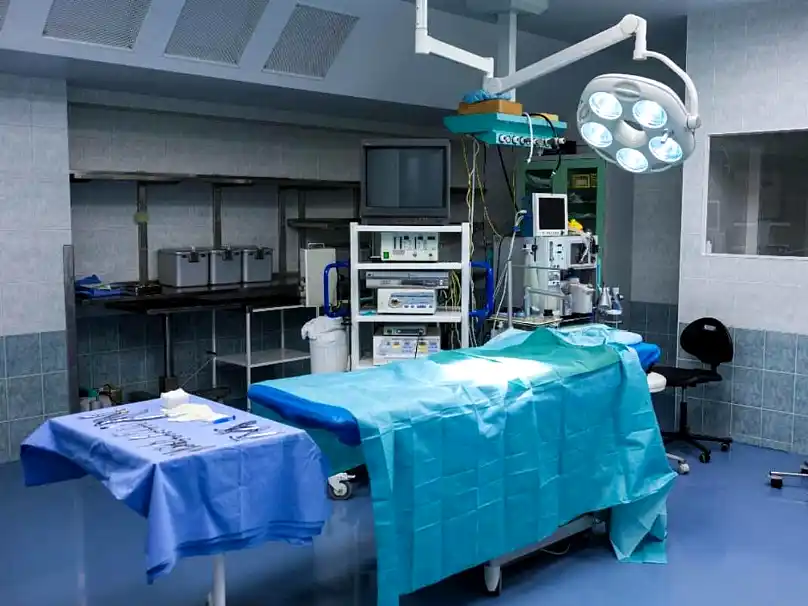
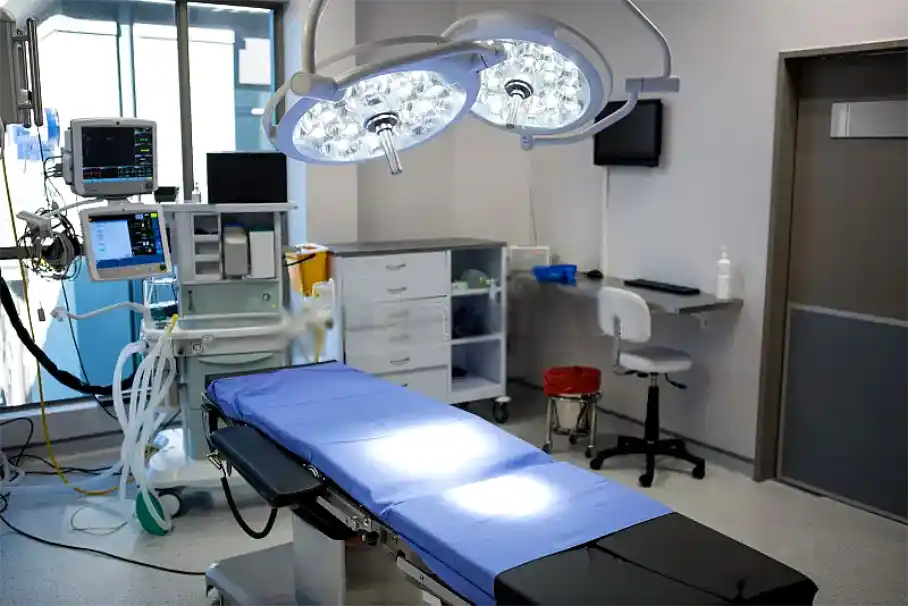
ANMAT actualizó su normativa y simplificó la importación de equipos médicos usados y reacondicionados, habilitando a hospitales y clínicas a acceder a tecnología sanitaria de calidad a menor costo.
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) puso en marcha una actualización normativa que moderniza y simplifica la importación de productos médicos usados y reacondicionados en la Argentina. La medida apunta a ampliar el acceso a tecnología sanitaria, reducir costos y facilitar la renovación de equipamiento en el sistema de salud.
Según informó el organismo, la reforma reemplaza regulaciones consideradas obsoletas y extiende el alcance del régimen a nuevos actores, más allá de importadores y fabricantes tradicionales. A partir de ahora, hospitales, clínicas y centros de diagnóstico también podrán gestionar directamente la incorporación de estos dispositivos, lo que representa un cambio significativo en el esquema regulatorio vigente.
Un nuevo marco para la importación de tecnología médica
El nuevo régimen definido por la ANMAT establece tres modalidades de importación para productos médicos registrados ante el organismo. La primera contempla equipos reacondicionados en el exterior; la segunda, dispositivos usados que, a criterio del importador, no requieren reacondicionamiento; y la tercera, equipos usados que ingresan al país para ser reacondicionados localmente.
En cada caso, la documentación exigida varía de acuerdo con el tipo de producto y su historial de uso. El objetivo, según explicó la agencia reguladora, es adecuar los requisitos a la realidad de cada equipo sin resignar estándares de seguridad y calidad.
Controles diferenciados según el nivel de riesgo
Uno de los ejes centrales de la actualización normativa es la implementación de un sistema de control diferenciado. ANMAT estableció que los productos de bajo riesgo tendrán una intervención previa reducida, lo que permitirá acelerar los tiempos de acceso al equipamiento. En contraste, los dispositivos de mayor complejidad o riesgo sanitario estarán sujetos a controles más estrictos y requerirán una autorización expresa del organismo.
Independientemente de la modalidad de importación, todos los productos deberán contar con certificados de reacondicionamiento o informes de verificación técnica. Estos documentos podrán ser emitidos por el fabricante original, por un servicio técnico local habilitado o por instituciones extranjeras radicadas en países considerados de alta vigilancia sanitaria.
La normativa aclara, además, que los productos médicos de uso único quedan excluidos de este régimen y tienen prohibida su importación bajo estas condiciones.
Acceso directo para hospitales y clínicas
Otro de los cambios relevantes es la ampliación de los sujetos habilitados para realizar el trámite. Con el nuevo esquema, clínicas, hospitales y centros de diagnóstico podrán gestionar directamente la importación de equipamiento médico usado o reacondicionado, sin necesidad de intermediarios.
Desde la ANMAT señalaron que esta apertura permitirá reducir costos, optimizar inversiones y facilitar que establecimientos de menor escala puedan modernizar su tecnología. El impacto esperado es una mejora en los diagnósticos y tratamientos, con un efecto positivo en la atención de los pacientes.
Antecedentes de flexibilización regulatoria
La reforma se inscribe en una serie de cambios impulsados por la ANMAT en los últimos meses. En octubre de 2025, el organismo avanzó en una flexibilización significativa para productos cosméticos y de higiene personal mediante la Disposición 7939/25, publicada en el Boletín Oficial.
Esa normativa simplificó el proceso de habilitación de establecimientos fabricantes e importadores de equipos, eliminó trámites burocráticos y digitalizó el procedimiento. A partir de ese esquema, las empresas pueden presentar una declaración jurada electrónica que certifica el cumplimiento de la normativa y de las Buenas Prácticas de Fabricación, habilitando la actividad de manera inmediata y sin fecha de vencimiento.
Una estrategia de reorganización institucional
En julio, el ministro de Salud de la Nación, Mario Lugones, explicó que estas reformas responden a una estrategia de refuncionalización de la ANMAT a nivel institucional. Según el funcionario, la intención es que la agencia concentre sus esfuerzos en el control de medicamentos, alimentos y dispositivos médicos, mientras que otras áreas, como la de productos cosméticos, migren hacia esquemas más descentralizados.
Lugones sostuvo que la reorganización busca recuperar eficiencia y confianza pública, evitando la superposición de funciones y la duplicidad de competencias regulatorias. En ese marco, remarcó la necesidad de fortalecer el rol técnico del organismo.
Cambios en la conducción de la ANMAT
En paralelo a estas reformas, la ANMAT atravesó recientemente un relevo en su conducción. Luis Fontana fue designado como nuevo titular del organismo, en reemplazo de Agustina Bisio, quien dejó el cargo por razones personales. Fontana, médico cirujano con trayectoria en el sector de la medicina prepaga, asume en un contexto de reformas orientadas a reforzar la continuidad institucional y el perfil técnico de una agencia reconocida por su prestigio internacional.
Con esta actualización normativa, la ANMAT busca equilibrar la agilización de procesos con el mantenimiento de altos estándares de control sanitario, en un intento por mejorar el acceso a tecnología médica y fortalecer el sistema de salud argentino.
 El diario
El diario